Calendrier scientifique Mars 2019
Comment la technologie de fluorocytométrie en flux sur les analyseurs de la série XN contribue-t-elle à différencier les échantillons de monocytose réactionnelle de ceux de la leucémie myélomonocytique chronique (CMML)?
En utilisant le paramètre de dispersion MO-WX combiné au ratio NEUT/MONO et MONO#, publié en tant que « score mono-displasie ».
En utilisant le paramètre de dispersion NE-WX combiné au ratio NEUT/MONO et MONO#, publié en tant que « score mono-displasie ».
Aucune aide n’est nécessaire ici. La CMML a toujours un MONO# > 3,0 x 10^9/L.
En utilisant le seul paramètre de dispersion MO-WX.
Congratulations!
That's the correct answer!
Sorry! That´s not completely correct!
Please try again
Sorry! That's not the correct answer!
Please try again
Notice
Please select at least one answer
Informations scientifiques générales
Leucémie myélomonocytique chronique (CMML)
La leucémie myélomonocytique chronique (CMML) est une pathologie maligne des cellules qui fabriquent le sang dans la moelle osseuse. C’est une maladie particulièrement variable, très similaire à divers types de cancers de la moelle osseuse et du sang présentant un trouble clonal des monocytes. L’OMS classe la maladie en néoplasmes myélodysplasiques et myéloprolifératifs (MDS et MPN). Chez les individus en bonne santé, les monocytes représentent respectivement moins de 1,0 x 109/L et 10 % des leucocytes. Chez les personnes souffrant de CMML, de trop nombreuses cellules souches se transforment en monocytes, mais toutes ne deviennent pas matures. Par conséquent, le sang périphérique développe une monocytose et des formes dysplasiques de neutrophiles et monocytes, tous deux caractéristiques d'une CMML, bien que la dysplasie puisse également être identifiée dans les globules rouges et/ou les plaquettes. Les cellules blastiques sont absentes dans 80 % des cas de CMML au plus, ce qui complique le diagnostic aux stades précoces de la maladie.
La CMML est une pathologie maligne rare dont l’âge médian du diagnostic se situe entre 65 et 75. On compte environ deux fois plus de patients que de patientes. Les signes et symptômes peuvent varier et incluent souvent de la faiblesse et de la fatigue dues à l’anémie, des pétéchies, des contusions et des saignements provoqués par la thrombocytopénie, des infections et une hypertrophie de la rate et du foie.
Certains patients chez qui une CMML est diagnostiquée étaient initialement venus passer un examen médical en raison d'une faiblesse physique, d'une infection ou de saignements inexpliqués. En général, un diagnostic de CMML n’est pas facile à confirmer. Les critères de diagnostic de l’OMS sont une monocytose persistante supérieure ou égale à 1,0 x 109/L, avec des monocytes représentant plus de 10 % des GB, une dysplasie affectant au moins une lignée dans le sang ou la moelle osseuse, moins de 20 % de cellules blastiques dans la moelle osseuse et/ou le sang, et/ou la présence d'une anomalie clonale. Le diagnostic de CMML nécessite un frottis sanguin minutieux et un examen de la moelle osseuse, ainsi que des analyses cytogénétiques, moléculaires et d’immunophénotypage (1).
La CMML est une maladie très hétérogène et il arrive que l'on passe à côté de ses formes latentes. Toutefois, un diagnostic précoce de CMML est nécessaire pour prévenir des conséquences graves telles que des infections et des complications hémorragiques, de même que pour retarder la transformation de la pathologie en leucémie myéloïde aiguë. Pour certains patients présentant des facteurs de pronostic favorables, un suivi sans traitement est parfois approprié. Pour d’autres, on peut envisager des soins de soutien ; des médicaments d’hypométhylation peuvent réduire les caractéristiques myélodysplasiques, et des agents cytoréducteurs sont utilisés pour contrôler les formes myéloprolifératives (2).
« Score mono-dysplasie »
En routine, les laboratoires sont souvent confrontés à des échantillons présentant un nombre accru de monocytes. La méthode utilisée actuellement pour examiner ces échantillons de façon plus approfondie est un examen du frottis sanguin effectué selon certains critères. Dans leurs critères, la Société internationale d’hématologie de laboratoire et le Groupe francophone d'hématologie cellulaire prennent en compte un MONO ≥ 1,5 x 109/L en tant que cut-off pour un examen de frottis de monocytose (3, 4). Comme l’OMS parle de monocytose dans les échantillons de CMML lorsque MONO ≥ 1,0 x 109/L et ≥ 10 % du nombre de globules blancs, certains cas de CMML ne seront pas détectés avec le cut-off susmentionné. Toutefois, la grande majorité des cas dans lesquels on identifie une monocytose relève de l’étiologie réactionnelle. Si l’on isole un nombre élevé de monocytes d'origine réactionnelle, l’examen du frottis n’apportera aucune autre information utile (5).
Un nouveau concept de flux de travail a été suggéré avec l’Extended IPU qui permet de se conformer aux critères plus stricts de l’OMS concernant la détection de la CMML (1), et soutient le choix des échantillons corrects de monocytose pour l’examen du frottis. Ce concept se fonde d'abord sur un « score mono-dysplasie » évalué et publié par Schillinger F et al. en 2018 (6). L'objectif de cette approche est d'optimiser le traitement des échantillons à analyser pour la monocytose, et ce faisant, de réduire les examens de frottis, tout en augmentant la sensibilité de la détection de CMML aux fins d'inspection ultérieure.
Les analyseurs Sysmex de la série XN utilisent la fluorocytométrie en flux dans le canal de mesure WDF pour différencier les sous-populations parmi les globules blancs. Après réaction du réactif, les cellules passent par un rayon laser et trois signaux de mesure sont détectés simultanément pour chaque cellule - signal de diffusion frontale (FSC), signal de diffusion latérale (SSC) et signal de fluorescence latérale (SFL). Ceci permet l’évaluation des caractéristiques morphologiques et de la fonctionnalité cellulaire.
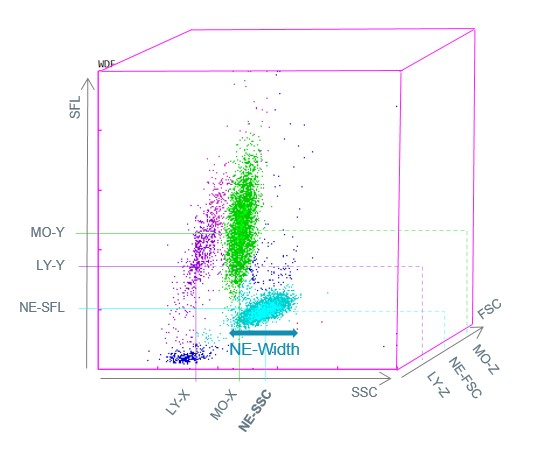
Le « score mono-dysplasie » se fonde sur des données en provenance du canal de mesure WDF, telles que le nombre de monocytes et de neutrophiles, ainsi que sur le paramètre de dispersion structurelle des neutrophiles (NE-WX). Le NE-WX reflète la dispersion structurelle des polynucléaires neutrophiles, car la displasie des neutrophiles est l’anomalie morphologique la plus fréquemment observée.
Le NE-WX se base sur la largeur de la diffusion latérale de la population de neutrophiles (largeur NE) par rapport à la position de sa diffusion latérale médiane (NE-SSC) (Ill. 1). C’est un paramètre extrêmement sensible pour identifier la coexistence des neutrophiles à peine granulaires et des neutrophiles normaux, en particulier dans les cas où les anomalies morphologiques sont difficiles à identifier au microscope. La combinaison de NE-WX, du ratio NEUT/MONO et MONO# dans un seul « score mono-dysplasie » s’est avérée être une nouvelle approche probante pour distinguer la CMML de la monocytose réactionnelle. La positivité du « score mono-dysplasie » a entraîné la mise en œuvre d’examens au microscope visant à rechercher des anomalies de CMML présentant une sensibilité de 96,7 % et une spécificité de 97,8 %, et a amélioré la détection de la CMML, tout en diminuant le nombre d’examens de frottis sanguins inutiles réalisés pour la monocytose chez les adultes (6).
Scattergrammes
Références
(1) Arber DA et al. The 2016 revision to the World Health Organization classification of myeloid neoplasms and acute leukemia. Blood 2016; 127:2391-2405.
(2) Patnaik MM et al. Chronic Myelomonocytic Leukemia: Focus on Clinical Practice. Mayo Clin Proc. 2016 Feb; 91(2):259-72.
(3) http://www.islh.org/web/consensus_rules.php
(4) Genevieve F et al. Smear microscopy revision: propositions by the GFHC. Feuillets de Biologie 2014; VOL LVI N° 317.
(5) Cornet E et al. Evaluation and optimization of the extended information process unit (E-IPU) validation module integrating the Sysmex flag systems and the recommendations of the French-speaking cellular hematology group (GFHC). Scand J Clin Lab Invest. 2016; 76(6):465.
(6) Schillinger F et al. A new approach for diagnosing chronic myelomonocytic leukemia using structural parameters of Sysmex XNTM analyzers in routine laboratory practice. Scand J Clin Lab Invest. 2018 May; 78(3):159-164.